今回はCritical Careより敗血症性脳症についての話です。
《本論文の一言まとめ》
敗血症性脳症の定まった診断は難しいが、原疾患の治療と並行して二次性脳損傷予防を意識した介入と脳症をきたしうる薬剤などへの対応が好ましいだろう
The spectrum of sepsis-associated encephalopathy: a clinical perspective
Crit Care. 2023 Oct 5;27(1):386.
Romain Sonneville, Sarah Benghanem, Lina Jeantin, et al.
疫学・臨床症状・危険因子
敗血症関連脳症(Sepsis-associated encephalopathy:SAE)は、敗血症により引き起こされる脳のびまん性の機能不全を特徴とする。
病態生理学は複雑だが、主なメカニズムの1つは炎症性サイトカインの放出により血液脳関門(Blood Brain Barrier:BBB)が破壊されることによる免疫細胞と炎症性メディエーターの脳への流入とされる。この炎症により脳の免疫細胞であるミクログリアを活性化させ、サイトカイン放出がさらに進み神経損傷をきたす。
SAEは全身の臓器障害や環境因子などの二次的な原因で誘発される可能性がある。
SAEはICUにおける脳症の最も一般的な原因と考えられている。またSAEの発生が短期死亡率と独立して関連していることも示されている。SAEの重症度は死亡率と相関しており、GCS 13-14程度の軽度の変化でも死亡リスクの増加に関連している。
ICUにおける脳症のデータはほとんどが一般集団を対象とした研究から得られている。敗血症患者を対象とした具体的な疫学研究は少なく、示されているSAEのリスク因子は以下の通り。
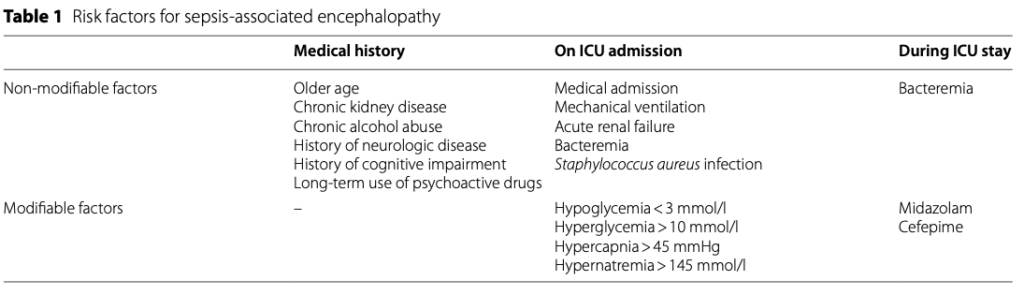
神経学的評価についても発熱、代謝異常、人工呼吸器管理のための薬剤投与などの修飾因子もあり、ICUにおけるSAEの評価は難しい。SAEは軽度のレベル低下から昏睡まで幅広い症状をとる。昏睡や活動低下が一般的で、興奮することは少ない。痙攣発作を起こすことは稀であり、その場合には脳実質の精査を行う必要がある。
画像診断
SAE患者でのCT検査の有用性に関するデータは限られている。非外傷性脳症患者におけるメタ解析では、症例の11%でCT異常所見が観察された。昏睡を含む脳幹症状を疑わせる症例では脳底動脈閉塞を除外するためにCTAを実施する必要がある。頭部MRIは局在性の所見、脳幹症状、新規の痙攣発作があり、原因となる因子(中毒、代謝異常、薬剤など)が存在せず、脳症症状が持続する場合に適応となる。その際には拡散強調(DWI)が虚血と炎症性変化の検出に最も感度が高いので、入れておくべき。
所見としては虚血性変化、白質病変、脳萎縮などがあり、SAE患者で認めることが多い。そして脳卒中や脳萎縮などが、死亡率や神経学的予後悪化に関連していることも報告されている。
脳波
EEGはSAEの確実な診断、NCSEの除外、予後予測において重要なツールとなる。問題点としては鎮静薬の影響で、容量に応じて背景脳波が徐波化する点である。EEGは感度は高いが、異なる脳症でも同様の異常パターンが現れる可能性があるためSAEの評価に特異的ではない。またEEGの解釈にばらつきがあるため、アメリカ臨床神経生理学会(the American Clinical Neurophysiology Society:ACNS)はこの解釈にばらつきが出ないように救急領域のEEGに特有の用語を導入した。
初期のEEG異常は臨床的な神経障害に先行する可能性や、脳症の重症度と相関している可能性がある。SAEにおける電気学的発作(ESz)の病態生理学については議論の余地があるが、神経毒性のある抗菌薬、代謝異常、AKIなどによる毒性物質の増加やてんかん誘発因子に関連している可能性がある。
血液バイオマーカー
神経損傷に関連する血液バイオマーカー、特にneuron-specific enolase(NSE)やneurofilament light(NfL)などが敗血症患者においてSAEの発症に関連するか予測するため評価された。特に利用しやすいのはNSEで、単施設研究ではあるがNSE>24.5mcg/LをカットオフとしたときのSAEに対する診断性能は感度54.2%、特異度83%であった。また研究によってはNSEの値と院内死亡率の関連が示されているが、示せなかったものもある。
SAEの診断に血液バイオマーカーを使用することは、診断に対する不確かさ、カットオフに対する閾値が定まっていないこと、バイオマーカーへのアクセスが限られていることなどから日常臨床で使用がしにくい点が課題とされている。そもそもSAEに関連する経路が敗血症と異なる可能性も示唆されており、この値をそのまま当てはめることは難しい。
管理
SAEの包括的な管理には集学的ケアが求められる。感染症の迅速な治療、蘇生が含まれる。せん妄の予防は最も重要であり、ABCDEFバンドルの実施は生命予後改善と意識障害の日数短縮に関連している。
SAEの診断のための簡略化されたアルゴリズムは以下の通り。
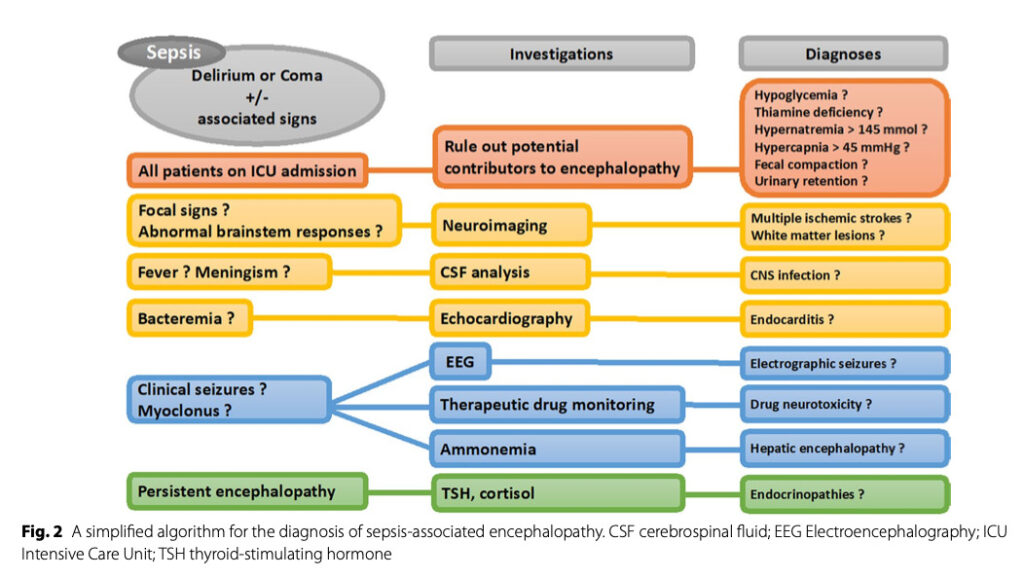
不穏による二次的な障害を防ぐために鎮静剤(プロポフォール、デクスメデトミジン)または抗精神病薬の使用が必要になる場合がある。ミダゾラムは脳症との独立した関連性があるため、投与は避けるべきである。腎障害は抗菌薬や睡眠導入剤などの様々な物質の蓄積に寄与する可能性がある。したがってβラクタム系抗菌薬、カルシニューリン阻害薬、抗真菌薬などの血中濃度をモニタリングすることも重要とされる。
SAEを管理するための多方面からのアプローチは以下の通り。
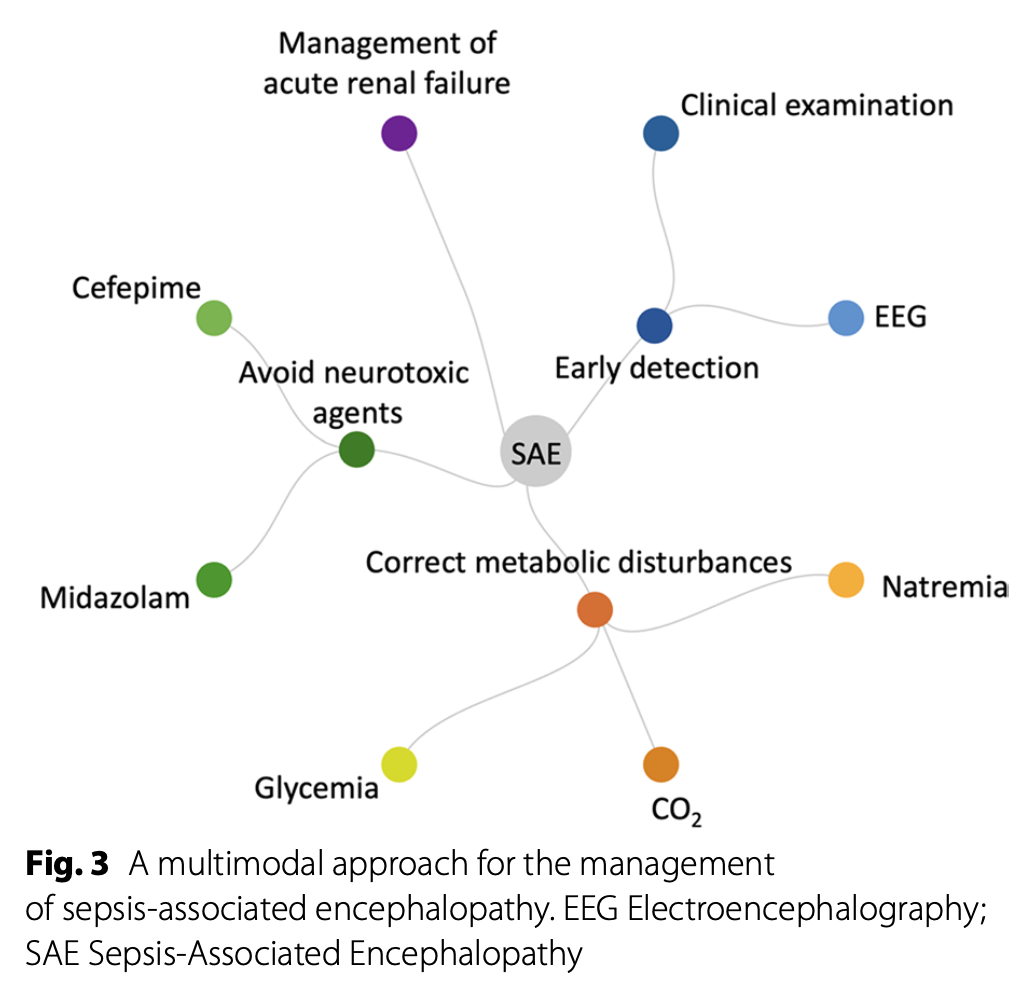
二次性脳損傷の原因は敗血症の発症時に頻繁に発生し、予後不良と関連している。原因には低血糖、高血糖、高CO2血症、高ナトリウム血症が含まれる。また低酸素、高酸素、貧血、低体温、高体温には特別な考慮が必要になる。現在の敗血症ガイドラインでは二次性脳損傷予防の推奨事項は書かれていないが、蘇生後管理ガイドラインなどと同様に以下の指標に注意して行うべきだろう。

さて、いかがでしたでしょうか。
基本的には原疾患の治療を粛々と行い、余計な薬剤使用などを避けることに尽きるかと思います。
抗菌薬では本文でも指摘されていましたが、特にCFPMの使用に注意が必要ですね。
感染症目線では良い薬剤ですが、全臓器をみる立場としては必ずしも、、、という印象です。
やはり意識に懸念がある人だと、このせいで呼吸器離脱ができずICU滞在が不必要に増えてしまう可能性もあるので、自分はかなり症例を選んで投与するようにしています。
詳しくは過去記事にまとめたので、ご参照ください。
今回はここまでです、ではでは。


コメント