今回は去年のESCから出された大動脈解離についてのreviewを読んでいきます。
致死的な疾患にも関わらず診断が難しく、救急医泣かせの疾患ですね。
ただその分きちんと診断評価できた時には専門科との信頼関係が築けると思いますので、しっかり勉強しておく必要があるでしょう。
Acute aortic dissection: evidence, uncertainties, and future therapies
Bartosz Rylski, Oliver Schilling, Martin Czerny
Eur Heart J. 2023 Mar 7;44(10):813-821.
PMID: 36540036 DOI: 10.1093/eurheartj/ehac757
大動脈解離は3層ある大動脈のうち、内膜が裂ける疾患である。
これにより追加の大動脈腔(偽腔)が形成される。
通常、患者は裂けるような放散する強い胸痛を自覚する。
上行大動脈を含む解離は、弓部や下行を含んでいなくても、A型大動脈解離(Type A)とされる。
仮に解離腔が弓部にはかかっているが、上行大動脈にかかっていない場合には、non-A non-B大動脈解離と表現する。
解離が下行のみであればB型大動脈解離(Type B)となる。
DeBakey分類によれば、以下のように区分される。
Type1:解離が上行から下行に及ぶもの
Type2:解離が上行に限局するもの
Type3a:解離が下行胸部大動脈に限局するもの
Type3b:解離が下行胸部から腹部大動脈にまで及ぶもの
解離のエントリーが上行大動脈にあるものは常にA型解離になり、進展を問わず外科的治療が選択肢になる。
逆行性解離はしばしば無冠尖を巻き込み、大動脈弁逆流をきたし、冠動脈閉塞(特に右)も起こしうる。
偽腔から心膜腔に交通することにより、心タンポナーデも起こすことがある。
B型大動脈解離は以下の3つに分けられる。
(i)複雑性
(ii)当初は非複雑性だが、解剖学的に複雑性への移行が推定される
(iii)非複雑性
なお複雑性の定義は脊髄、腸管、腎臓、四肢への血流障害を指す。
さらに言えば、血性心嚢水の存在、血管の破裂、大動脈最大径が40mmを超える、痛みが持続しているというのは複雑性と判断させる。
また大動脈解離を複雑性にする解剖学的な因子は最低でも2つはある。
それは解離のエントリーが小湾側にある場合と左鎖骨下動脈から近く(<2cm)にある場合である。
小湾側に解離があると大湾側と違って解剖学的にエントリーが広がることを防ぐもの(頸部分枝)がなく、逆行性解離のリスクが上がる。
・A型大動脈解離
長年、上行大動脈置換術がA型大動脈解離の治療選択肢とされていた。
解離の分類によって治療方針が異なる可能性もあり、新たにtype entry malperfusion(TEM)分類が提唱された。
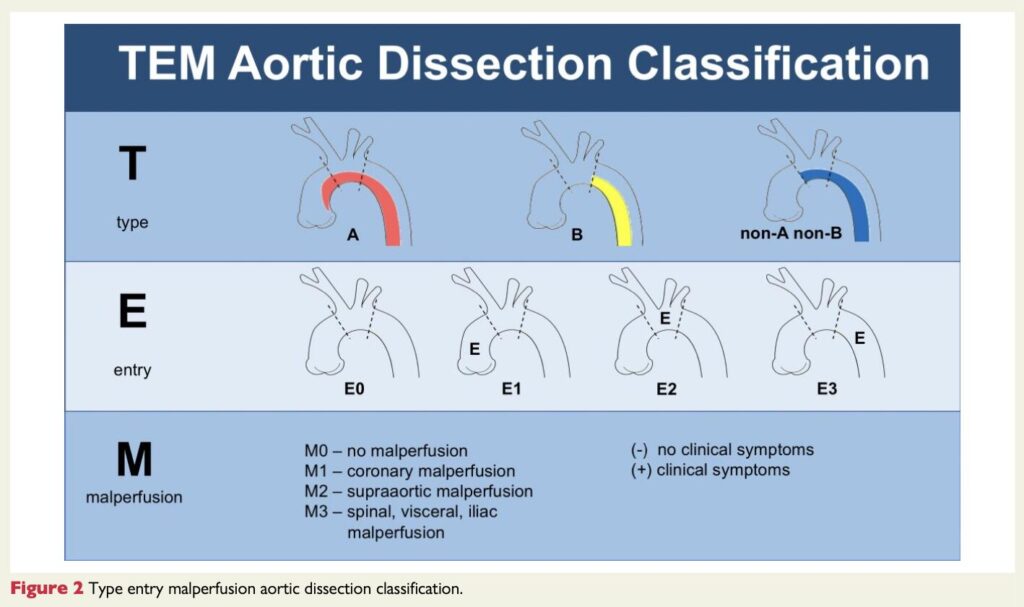
TEM分類は解離の解剖学的形態とmalperfusionの状態により決まり、Stanford分類にnon-A non-Bを追加し(T)、エントリー部位(E)、malperfusionの種類(M)を反映させる。
具体的には以下の通り
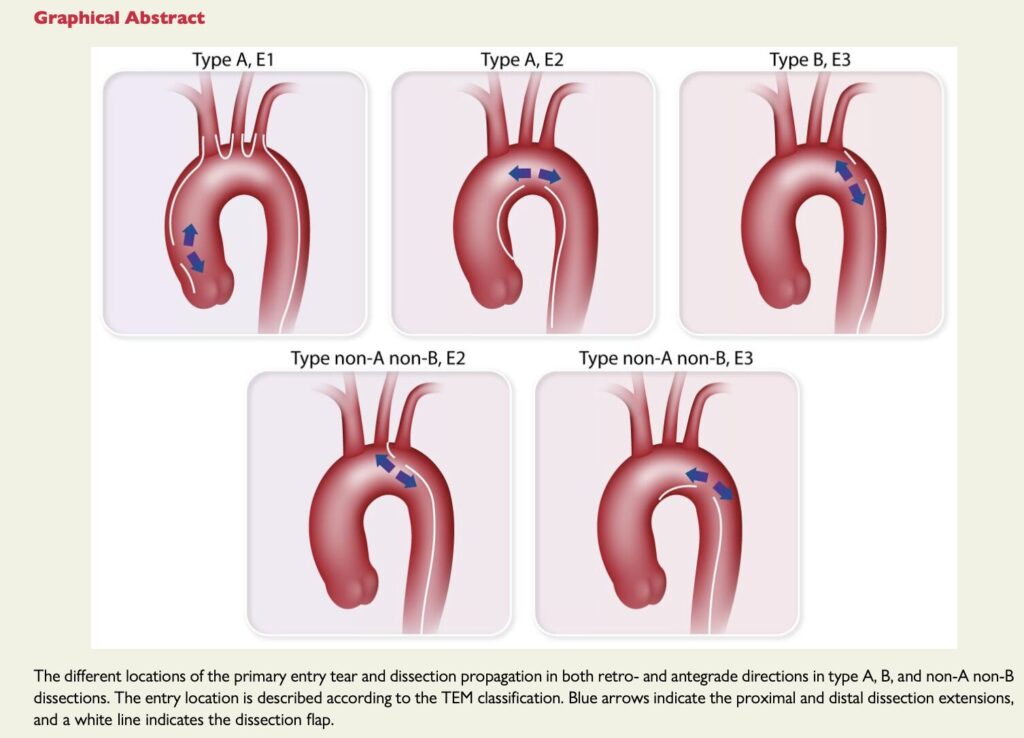
E0:エントリー不明
E1:上行にエントリー
E2:弓部にエントリー
E3:下行にエントリー
M0:malperfusionなし
M1:冠動脈にmalperfusionあり
M2:頚部動脈にmalperfusionあり
M3:脊髄、腹部、腸骨動脈にmalperfusionあり
そしてmalperfusionが臨床的に存在するなら+、しなければ-を画像所見に付け加える。
多くのTEM Type A E1 M0は上行置換の恩恵を受ける一方で、TEM Type A E2 M3 +は末梢臓器のためにもエレファントトランクを用いた弓部置換術が必要になる場合がある。
A型大動脈解離の予後は5%から75%と大きく幅があり、過去の神経傷害や臓器灌流不全、基礎疾患によるところが大きい。
A型大動脈解離の30日死亡率を予測するスコアリングシステムにGerman Registry for Acute Type A Aortic Dissection(GERAADA)がある。
これには年齢、性別、術前の心停止、過去の心臓手術歴、事前の挿管、カテコラミン使用、AR、malperfusionの状態、神経状態、解離の広さが含まれる。
・non-A non-B大動脈解離
頻度としては全体の7-11%を占めていて、弓部にエントリーがあるもの(E2)と下行大動脈にエントリーがあるもの(E3)で半分ずつとなる。
面白い現象として小湾側にエントリーがあると、頚部3分枝が無いので解剖学的に逆行性のA型大動脈解離になりやすい。
緊急での手術となるのは、大動脈破裂と末梢臓器のmalperfusionである。
実のところを言えばnon-A non-Bに対する緊急手術は意見の分かれるところであり、近位側のエントリーを残してしまうと後日にA型大動脈解離をきたしてしまう。
それはTEVARで治療を行った場合も同様であり、特にnon-A non-B E2患者においては避けるべきとされている。
・B型大動脈解離
常に手術を必要とするA型と異なり、薬物治療のみで経過を見ると長らく考えられていた。
しかし昨今の知見では比較的急性期でも外科的介入を検討する症例があることが報告されている。
急性期(発症から14日以内)での外科的介入の最も一般的な理由としては、末梢臓器のmalperfusion、逆行性の解離の進展、痛みの持続がある。
以降の外科的介入は、多くは大動脈径による。
INSTEAD trialとINSTEAD-XL trialではTEVARの有用性が示された。
早期のTEVARのメリットとしては真腔の復帰と偽腔の血栓化が進むことが挙げられる。
大動脈径や瘤のリスク因子には直径40mm以上、偽腔径22mm以上がある。
・今後の展望
大動脈解離で注意することはエントリーがどこかと、逆行性ないし順行性の進展である。
TEVARは近位側に十分な距離が必要であり(landing zone)、そのためA型大動脈解離における使用は限られている。
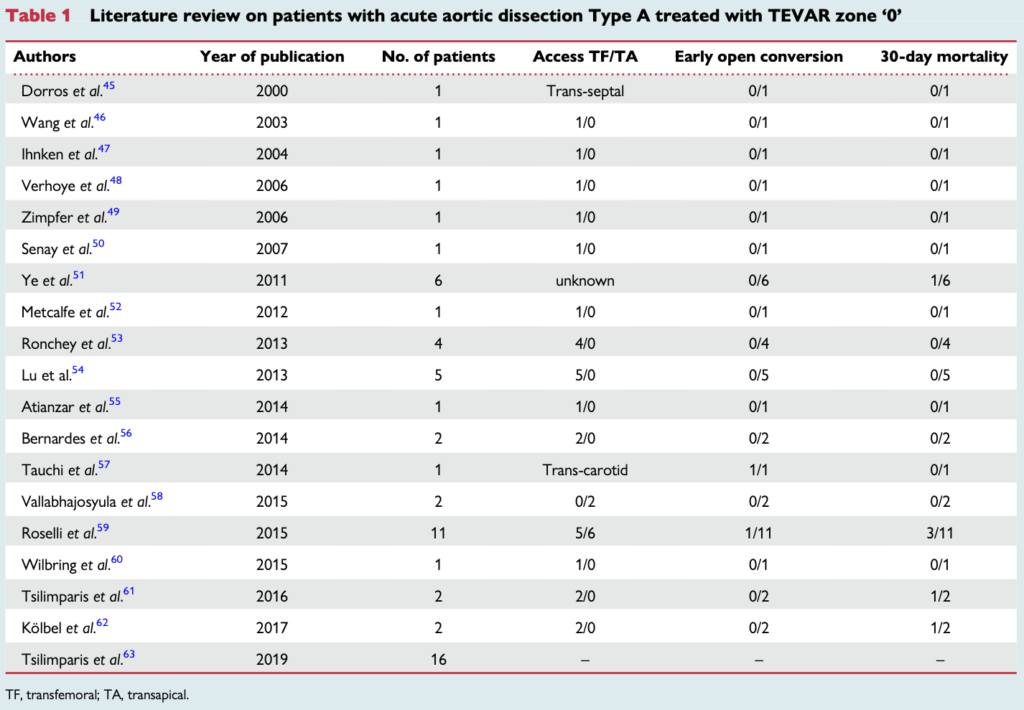
このように治療報告はでているが、まだ数えるほどに留まっており定まった知見や適応はない。
いかがだったでしょうか。
大動脈解離は非専門医としては診断学がとても重要かと思います。
見逃しが死に直結する疾患になりますので。
ただ診断後の分類も少し変わってきていることを知っていると、より専門科と話すときに良いかもしれません。
ただ過去には解離かつSTEMIの時にどちらを優先するか?という記事も書きましたが、管理もとても難しいですよね。。。
ちなみに当院においてA型大動脈解離で速やかに血管オペに行かないのは2パターンです。
①腸管虚血
こちらはESC2022にも書いてありますが、唯一先に虚血解除を考えるmalperfusionです。
これは致死的になるので、先に開腹してから血管直す事もあります。
ただ結局3-4時間はかかってしまうのでそこが難点で、開腹してSMAとかに順行性シース刺して送血するというワザもあるようです。
ただこれも解離してるとこに送血するので、真腔捉えるの難しく簡単ではありませんね。
②心筋虚血
前述の過去記事の通りですが、ESCやAHAのガイドラインには記載ないものの本邦ガイドラインには触れられています。
致死的不整脈リスクもあるので、確かに解除する時間があるならトライしたい気持ちもありますね。
ただ解離で血栓化してる事もありPCIが難渋することが多いようです。
当院では右冠動脈を噛んでいるmalperfusionは無視、左を噛んでたらPCI先行というプラクティスになっています。
日本はPCI先行の報告がパラパラあり、カテーテルアクセスが良いからでしょう。
当院もカテアクセスが早いため、PCIトライを選択肢に残しています。
また今後の展望としてはTEVARでA型大動脈解離を治療する報告も出始めており、医療の進歩を強く感じます。
少し脇に逸れましたが本日はこの辺で。
ではでは。


コメント